Im Oktober wurde der erste Patient in eine klinische Phase-3-Studie zur Untersuchung der Sicherheit und Wirksamkeit eines polyklonalen Anti-SARS-CoV-2-Hyperimmunglobulin (H-IgCoVIg Hyperimmun)-Medikaments aufgenommen. Mit dem Hyperimmunmedikament werden in der Studie Patienten mit schweren Komplikationen von COVID-19 behandelt. (Lesen Sie hier die vollständige Pressemitteilung).
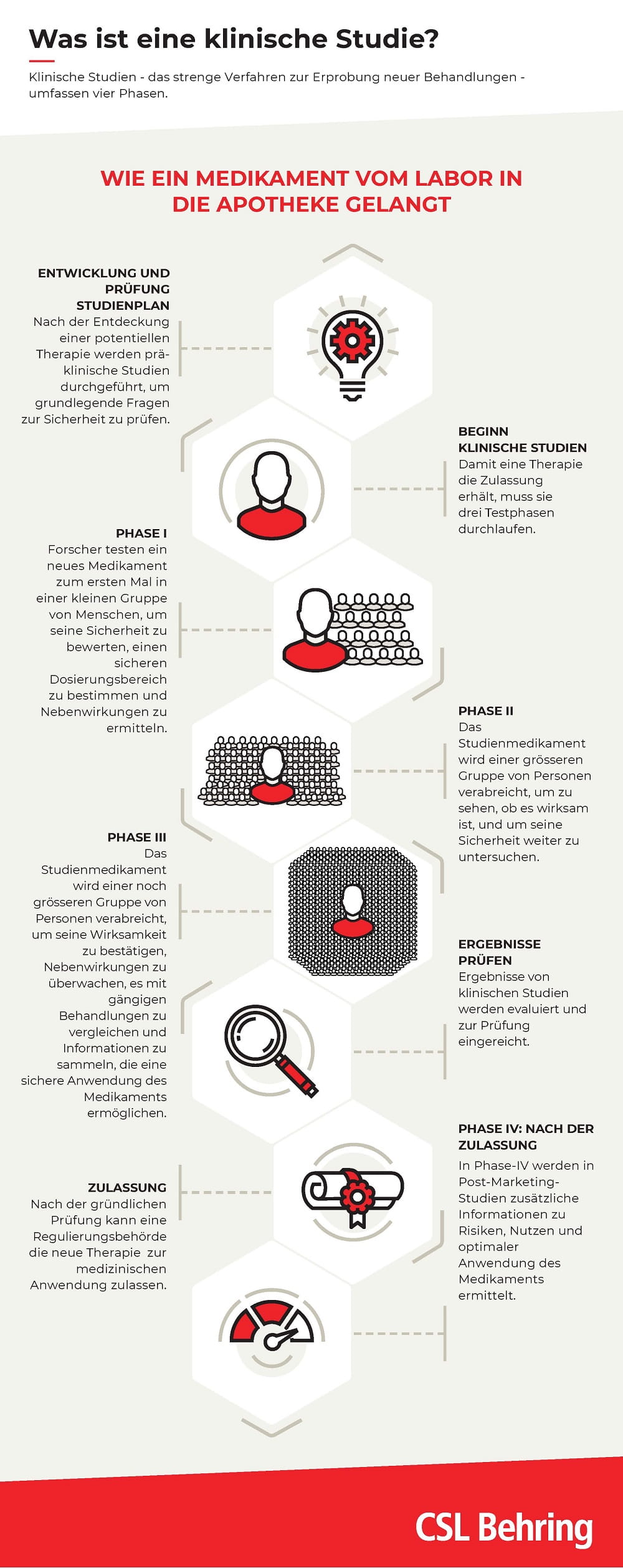
Klinische Studien - das strenge Verfahren zur Erprobung neuer Behandlungen - umfassen vier Phasen (s. Grafik). Jede Phase einer klinischen Studie dient einem spezifischen Zweck. Doch Phase III ist besonders wichtig. Denn in Phase-III-Studien wird das Studienmedikament einer grösseren Gruppe von Personen verabreicht. Diese ist von verschiedenen Faktoren abhängig, z.B. von der Art der Krankheit oder dem therapeutischen Effekt. So können in der Phase III schnell mehrere Tausend Patienten notwendig sein, um die Wirksamkeit des Medikaments zu bestätigen, allfällige Nebenwirkungen zu überwachen, es mit gängigen Behandlungen zu vergleichen und Informationen zu sammeln, die eine sichere Anwendung des Medikaments ermöglichen.
Beschleunigtes Verfahren dank bereits geprüfter Herstellungsprozesse
Normalerweise nehmen die ersten drei Phasen der klinischen Testung eines neuen Medikaments sehr viel Zeit in Anspruch, und es dauert Jahre bis zur Marktzulassung. Doch im Falle der Entwicklung des CoVIg Hyperimmuns kann auf bereits geprüfte Produktionsverfahren und bereits durchgeführte klinische Studien zurückgegriffen werden, weil das neue CoVIg Hyperimmun auf dieselbe Art und Weise hergestellt werden kann wie ein bereits auf dem Markt erhältliches Produkt, welches bei Immunmangelerkrankungen zum Einsatz kommt.>Aus diesem Grund und dank der entsprechenden Sondergenehmigung der FDA (U.S. Food & Drug Administration) sowie der Unterstützung des U.S. National Institutes of Health (NIH) war es möglich, die klinischen Phasen I und II zu überspringen und direkt zur entscheidenden Phase III vorzurücken, und damit im Kampf gegen das Coronavirus wertvolle Zeit zu gewinnen. Das NIH ist eine Behörde des US-amerikanischen Gesundheitsministeriums und die wichtigste Behörde für biomedizinische Forschung in den USA.
Was ist eine klinische Studie?
Die vier Phasen der Neu-Entwicklung eines Produktes sind weltweit dieselben (s. Grafik). Die daraus gewonnenen Daten werden von Gesundheitsbehörden genutzt, um über die Zulassung neuer Therapien im jeweiligen Land zu entscheiden.